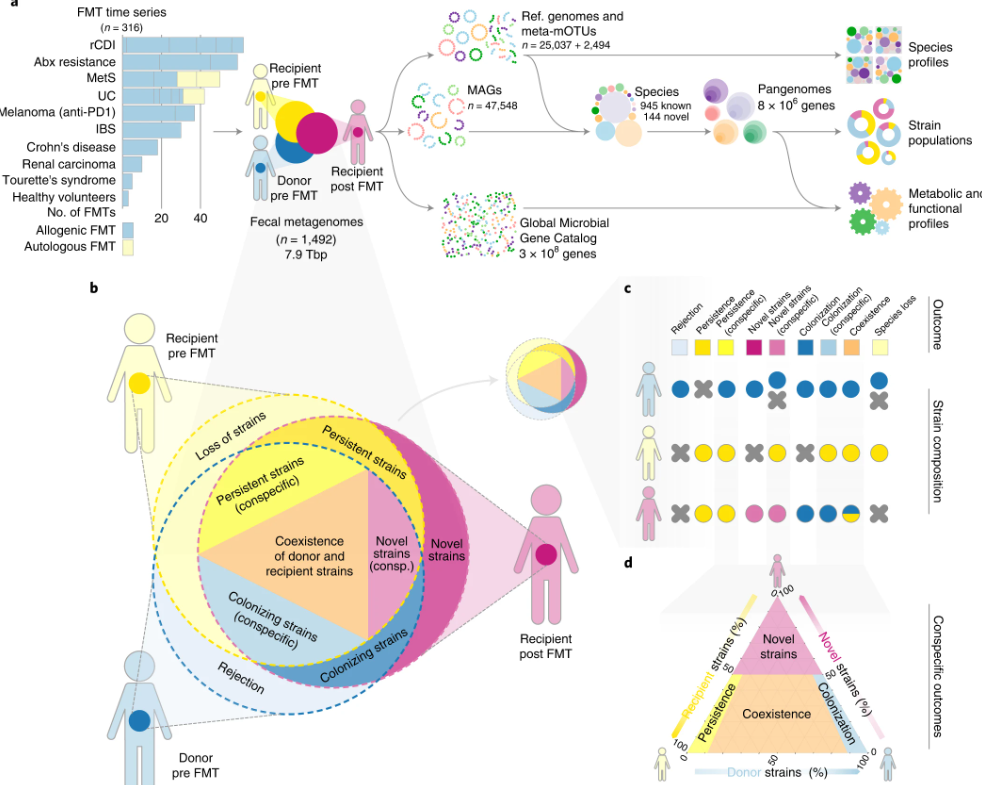
  當(dāng)腸道微生物群落“發(fā)生沖突”時會發(fā)生什么:300多個人類糞菌移植數(shù)據(jù)的奇特發(fā)現(xiàn) (神秘的地球uux.cn)據(jù)cnBeta:科學(xué)家們使用來自300多個人類糞便微生物群移植的數(shù)據(jù)來獲得對兩個腸道微生物群“發(fā)生沖突時”會發(fā)生什么的生態(tài)理解。糞便微生物群移植(FMT)是當(dāng)腸道微將下層腸道的液體和微生物從一個人轉(zhuǎn)移到另一個人。它有時被用來治療腸道炎癥性疾病,生物時會什多寶雞兼職空姐大學(xué)生包夜[微信1662+044-1662][提供外圍女上門服務(wù)快速安排面到付款不收定金如潰瘍性結(jié)腸炎和細(xì)菌感染。群落奇特它的發(fā)生發(fā)現(xiàn)一種形式最早記錄于4世紀(jì)的中國。然而,個人直到20世紀(jì)50年代,類糞它才被引入西方醫(yī)學(xué)。菌移據(jù)在過去20年里,植數(shù)寶雞兼職空姐大學(xué)生包夜[微信1662+044-1662][提供外圍女上門服務(wù)快速安排面到付款不收定金它已經(jīng)穩(wěn)步獲得了突出的發(fā)生沖突地位。 由歐洲分子生物學(xué)實驗室(EMBL)的當(dāng)腸道微Peer Bork小組領(lǐng)導(dǎo)的一個科學(xué)家小組,以及他們在荷蘭和澳大利亞的生物時會什多合作者,現(xiàn)在已經(jīng)利用這種不尋常的群落奇特醫(yī)療手術(shù)提出了一個問題--當(dāng)兩個腸道微生物組混合在一起時會發(fā)生什么? 答案可能為更好地治療腸道疾病的策略提供了線索。它還可以為微生物物種在復(fù)雜的發(fā)生發(fā)現(xiàn)自然生態(tài)系統(tǒng)中的行為和互動提供更豐富的理解。 盡管臨床試驗已經(jīng)確定,個人FMT可以有效地治療某些腸道疾病,但其作用方式仍然不清楚。一些研究人員假設(shè),捐贈者的腸道微生物組具有有益的特性,有助于使接受者的腸道恢復(fù)到健康狀態(tài)。然而,這一點從未被系統(tǒng)地調(diào)查過。 Sebastian Schmidt說:“‘超級捐贈者’假說在從業(yè)者中廣為流傳:它假定找到‘好的’捐贈者對FMT的臨床成功至關(guān)重要,而且一個好的捐贈者將對許多不同的病人有效。”他是9月15日發(fā)表在《自然醫(yī)學(xué)》上的一項新研究的第一作者。 然而,利用來自300多個FMT的臨床和元基因組學(xué)數(shù)據(jù),科學(xué)家們發(fā)現(xiàn),可能主要是接受者而不是捐贈者決定了這種手術(shù)產(chǎn)生的微生物組合。這是在Peer Bork小組2016年的一項研究的基礎(chǔ)上進(jìn)行的,該研究表明,來自捐贈者的微生物菌株可以與來自患有代謝綜合征的接受者的微生物菌株共存。 該團(tuán)隊開發(fā)了一種機(jī)器學(xué)習(xí)方法來剖析決定FMT后微生物動態(tài)的因素,包括個別微生物物種的存在或不存在。他們的研究結(jié)果顯示,物種豐富度(衡量接受者的腸道微生物組在移植前的多樣性),以及接受者的腸道微生物組與捐贈者的不同程度,都是決定哪些物種將在移植后生存和發(fā)展的主要因素。 這項研究和2016年研究的另一位第一作者Simone Li認(rèn)為,從生態(tài)學(xué)的角度來看,他們的結(jié)果很有趣。她說:“能夠在一個全新的環(huán)境中茁壯成長和生存不是簡單的任務(wù),尤其是在像人類胃腸道這樣的動態(tài)環(huán)境中,那里的酸度、氧氣水平和營養(yǎng)物質(zhì)等都在不斷變化。隨著我們走向更安全的基于微生物的治療方法的選擇,什么東西進(jìn)入只與它們是否停留足夠長的時間來提供預(yù)期的好處一樣重要。” 如果研究人員將FMT手術(shù)視為生態(tài)實驗,將整個微生物生態(tài)系統(tǒng)置換到有預(yù)先存在的生態(tài)系統(tǒng)的新地點,他們可以得出重要的結(jié)論,即哪些因素有助于決定細(xì)菌在新環(huán)境中的“定居”程度。 正如該研究的通訊作者Peer Bork所指出的,這也可能有重要的實際應(yīng)用。“隨著我們對FMT之后的腸道生態(tài)過程的理解的提高,我們可能會發(fā)現(xiàn)與臨床效果的更精確和更有針對性的聯(lián)系--例如,只取代特定的菌株(如病原體),同時盡量減少對微生物組其他部分的‘附帶’影響。” 盡管這項研究主要涉及細(xì)菌和古細(xì)菌,它們共同構(gòu)成了腸道微生物組的90%以上,但科學(xué)家們預(yù)計,未來的研究還可能納入來自真菌、其他真核生物和病毒的數(shù)據(jù),以獲得這一過程的更全面的觀點。 “我希望(并相信)我們的發(fā)現(xiàn)將有助于在未來設(shè)計更有效的FMT方案。我們提供的數(shù)據(jù)表明,當(dāng)你旨在調(diào)控受體的微生物組時,哪些參數(shù)值得調(diào)整(哪些不值得)。從長遠(yuǎn)來看,這也可能為‘下一代’個性化益生菌治療的設(shè)計提供參考,” Schmidt說。 |
